Introducción
La neuroinflamación está involucrada en la fisiopatología de diferentes trastornos neurológicos, en particular la enfermedad de Alzheimer (EA) y la enfermedad de Parkinson (EP). Las alteraciones en la barrera hematoencefálica pueden permitir la entrada al sistema nervioso central de linfocitos periféricos, los cuales pueden participar en la patología de las enfermedades.
Objetivo
Evaluar el perfil de linfocitos periféricos en pacientes con EA y EP y su asociación con la enfermedad y su progresión.
Métodos
Se incluyeron 20 pacientes con EA, 20 pacientes con EP y un grupo de individuos sanos. Diez de los pacientes con EA y 12 de los pacientes con EP fueron evaluados una segunda vez de 17 a 27 meses después del inicio del estudio. Las subpoblaciones de linfocitos y su estado de activación se determinaron mediante citometría de flujo. Todos los pacientes fueron evaluados neurológicamente utilizando escalas validadas internacionalmente.
Resultados
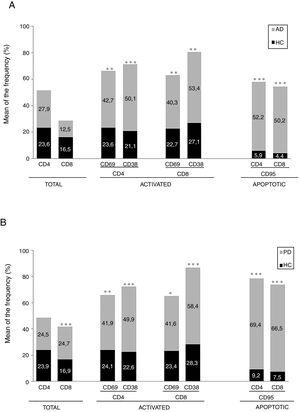
Los pacientes con EA y EP mostraron un aumento significativo en los niveles de linfocitos activados, linfocitos susceptibles a la apoptosis, células T de memoria central y células T y B reguladoras con respecto a los sujetos sanos. A medida que las enfermedades progresaron se observó una disminución significativa de las células activadas (CD4+ CD38+ y CD8+ CD38+ en EP y EA; CD4+ CD69+ y CD8+ CD69+ en EP), de las células T susceptibles a la apoptosis y de algunas poblaciones reguladoras (CD19+ CD5+ IL10+ en EP y EA; CD19+ CD5+ IL10+ FoxP3+, CD4+ FoxP3+ CD25+ CD45RO+ en EP). En pacientes con EA la progresión de la enfermedad se asoció con porcentajes más bajos de CD4 + CD38 + y mayores porcentajes de células CD4 efectoras al comienzo del estudio. Se observaron diferencias significativas entre ambas enfermedades.
Conclusiones
Este estudio proporciona evidencia de cambios en los fenotipos de linfocitos periféricos asociados a EA y EP y a su gravedad. Teniendo en cuenta la comunicación efectiva sangre-cerebro, nuestros resultados abren nuevas vías para explorar terapias de inmunomodulación para tratar estas enfermedades.