Introducción
En diciembre de 2021 comenzó en España la campaña de vacunación contra la COVID-19 en niños de 5 a 11años. A pesar del buen perfil de seguridad de la vacuna (Comirnaty®) en los estudios precomercialización, suscitó cierta incertidumbre en la población por su rápida implementación y tecnología novedosa, llevando a los padres incluso a dudar sobre la vacunación de sus hijos. Existen pocos estudios poscomercialización en condiciones reales para evaluar la seguridad y respaldar decisiones clínicas y epidemiológicas fundamentadas.
Objetivo
Evaluar la incidencia y las características de las reacciones adversas tras la vacunación pediátrica frente a la COVID-19.
Material y métodos
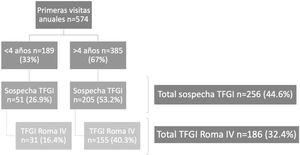
Estudio observacional, ambispectivo y descriptivo, realizado en un hospital terciario. Se incluyeron 2.126 niños de 5 a 11años. Se recogieron reacciones adversas a medicamentos (RAM) mediante entrevistas telefónicas, revisión de historia clínica y registros institucionales, evaluadas por un comité experto según criterios de causalidad y gravedad preestablecidos.
Resultados
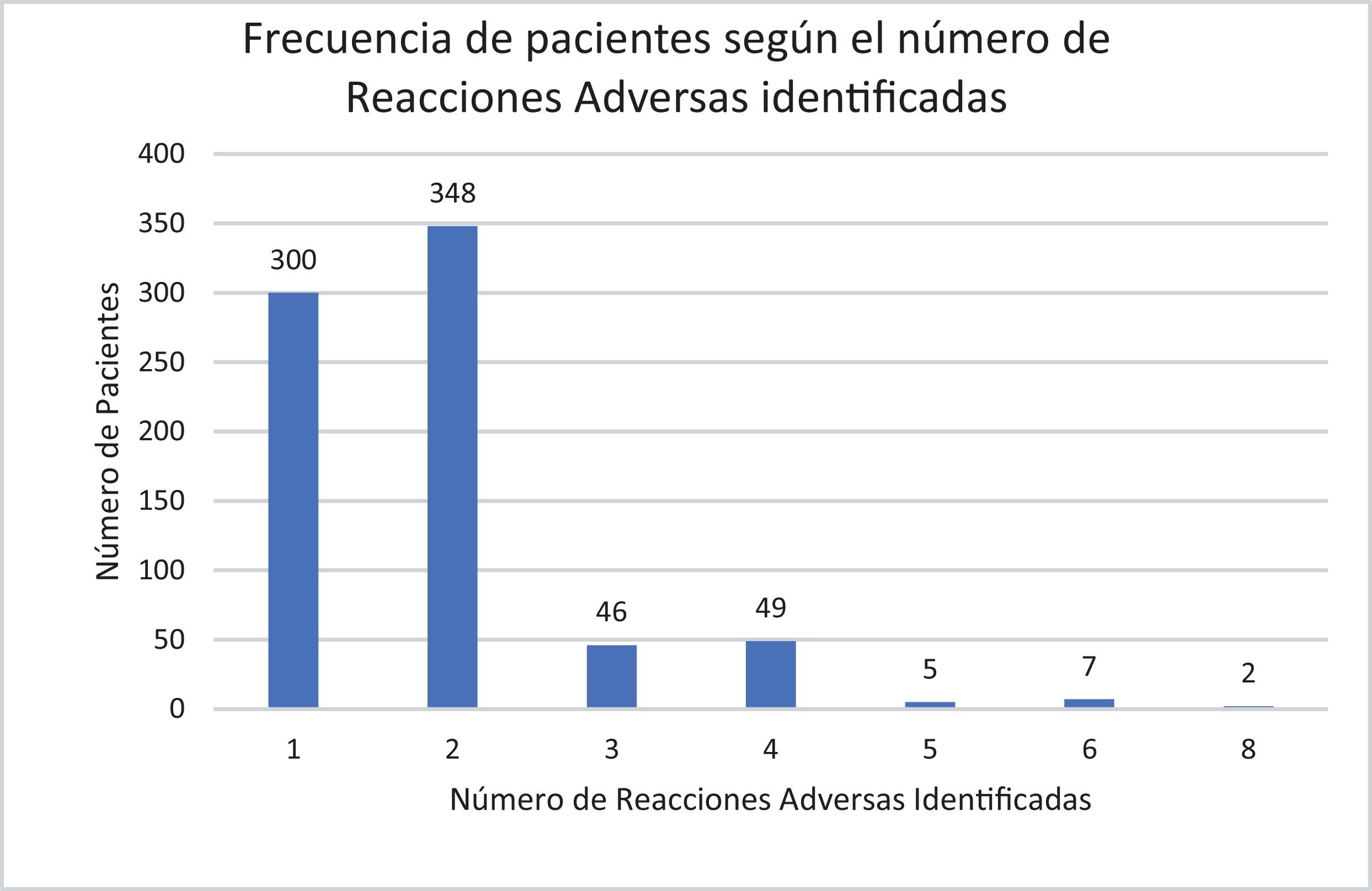
El 35,6% presentaron al menos una RAM, con un total de 1.437 reacciones. La mayoría fueron leves (99,5%) y de resolución espontánea. Solo un caso fue clasificado como grave. Las RAM más frecuentes fueron dolor en el lugar de inyección (57,1%), fiebre (11,1%) y cefalea (5,7%). No se identificó mayor reactogenicidad tras la segunda dosis. El 65,1% de las RAM fueron clasificadas como «definidas» o «probables».
Conclusiones
La vacuna Comirnaty® mantiene un perfil de seguridad favorable en población pediátrica en condiciones reales, con predominio de RAM leves, autolimitadas y con escasa necesidad de atención médica.