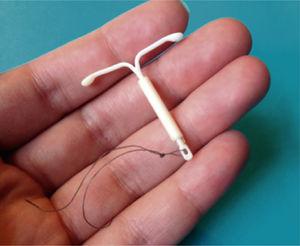
Los dispositivos intrauterinos hormonales de levonorgestrel son métodos anticonceptivos seguros y eficaces. Al igual que los medicamentos convencionales, una vez expirada la patente, las autoridades regulatorias de salud pueden aprobar el registro de productos similares. El objetivo de ello es disminuir los costos, considerando el elevado precio del producto original. Este tipo de productos están regulados y se aplican requisitos generales similares a los medicamentos tradicionales para demostración de seguridad y eficacia. Las propiedades mecánicas únicas del producto de referencia plantean un gran desafío a los productos similares. El presente artículo analiza de manera comparativa las características de los diversos sistemas intrauterinos hormonales de levonorgestrel, disponibles en el mercado. La autoridad sanitaria y los diversos centros clínicos deben considerar que en este tipo de productos no hay, hasta la fecha en el mundo, genéricos intercambiables y que por lo tanto, se debe decidir la intercambiabilidad de éstos sobre la base de estudios de bioequivalencia in vivo, luego de la demostración de equivalencia farmacéutica in vitro, tal y como sugiere la FDA, o en su defecto deberían ser registrados como productos nuevos, con estudios clínicos apropiados que demuestren seguridad y eficacia.